国际法规信息合集(二)
美国发布《实验室开发测试(LDT)法规》
2024年7月2日,美国发布《实验室开发测试(LDT)法规》。该法规明确了体外诊断产品 (IVD) 受联邦食品、药品和化妆品法案 (FD&C 法案) 管理。该法规旨在帮助小型实体遵守适用的医疗器械法规,逐步取消美国食品和药物管理局(FDA)对LDT的一般执法自由裁量权方法,以便实验室生产的IVD采用与其他IVD相同的执法方法。
来源:技贸措施公共服务平台
韩国明确变更标示、广告的营业者等费用支援范围
2024年7月2日,韩国食品药品安全部(MFDS)修改了《食品等的标示、广告相关法律实施规则》部分内容。
本次修改的主要内容包括:规定毒品类及使用类似表现形式的标示、广告的具体内容;根据建议,明确对拟变更产品标识、广告的营业者等的费用支援范围包括变更招牌、菜单及包装材料所需的费用等。
来源:食品伙伴网
澳大利亚修订治疗用品中防晒霜的规定
2024年6月7日,澳大利亚联邦公报发布F2024L00657号公告,批准修订2024年治疗用品(防晒霜)修正案,主要内容:
(1)制订澳大利亚/新西兰标准AS/NZS2604:2021《防晒产品-评估和分类》标准;
(2)有防晒霜的唇部和的有色底霜和粉底产品必须不含禁用的药物,要在标签注明防护因素并符合广谱产品的性能要求;
(3)有防晒霜的用于皮肤的保湿护肤产品(包括抗皱、抗衰老和美白产品)必须不含禁用的药物;要在标签注明防护因素;宣称防晒系数不得超过UVAPF15,保存期限超过36个月的应标明保质期;包装容量不超过300ml或300g;除宣称可抗与日晒有关的过早衰老外,不得宣称其它治疗效果(包括与皮肤癌有关的声明);
(4)含有防晒成分的日光浴护肤产品(如油、霜、凝胶、不含防晒成分的美黑产品和晒后护理产品)防晒系数至少UVAPF4不超过UVAPF15;要在标签注明防护因素并符合广谱产品的性能要求;宣称防晒系数不得超过UVAPF15,保存期限超过36个月的应标明保质期;包装容量不超过300ml或300g;除宣称可抗与日晒有关的过早衰老外,不得宣称其它治疗效果(包括与皮肤癌有关的声明)。
该公告自2024年7月1日起生效。
来源:技贸措施公共服务平台
马来西亚修订化妆品管制法规
2024年6月19日,马来西亚国家药品管理局发布2/2024号公告,修订《化妆品管制法规》。主要内容为:化妆品限制使用的成分清单中新增水杨酸等4种物质,并规定使用要求,具体如下表。该公告自发布之日起生效。
|
物质名称 |
使用产品范围 |
最大使用浓度 |
备注 |
|
水杨酸 (salicylic acid) 以外用途) |
淋洗类发用产品 |
3% |
2025年11月21日起实施 |
|
其它化妆品(不包括身体乳液、眼影、睫毛膏、口红、非喷雾型除臭剂) |
2% |
||
|
身体乳液、眼影、睫毛膏、口红、非喷雾型除臭剂 |
0.50% |
||
|
吡啶硫酮锌(zinc pyrithione) |
驻留类发用产品 |
0.1% |
2026年5月14日起实施 |
|
淋洗类发用产品 |
1% |
||
|
硅酸铵银锌铝(ammonium silverzincaluminum silicate) |
粉底 |
1% |
2025年5月8日起实施 |
|
除臭剂 |
1% |
||
|
酸性黄3号(Acid yellow 3) |
非氧化性染发剂 |
0.50% |
2026年5月14日起实施 |
来源:技贸措施公共服务平台
欧盟化妆品法规将禁用20余种CMR(致癌、致突变或生殖毒性)物质
2024年6月24日,欧盟委员会向世界贸易组织(WTO)递交G/TBT/N/EU/1070号通报,拟对(EC) No 1223/2009(即欧盟化妆品法规)附录Ⅱ(禁用)和附录Ⅲ(限用)进行修订。
主要新增了 (EC) No 1272/2008(即欧盟CLP法规)附录Ⅵ在2023年10月修订时明确的致癌、致突变或生殖毒性(CMR)物质,法规预计于2025年第3季度通过并实施。

G/TBT/N/EU/1070号通报
修订背景
2023年10月19日,欧盟委员会发布法规(EU) No 2024/197,拟对(EC) No 1272/2008(即欧盟CLP法规)附录Ⅵ进行修订,包括引入或更新一系列物质的统一分类和标签,预计于2025年9月1日生效。
本次化妆品法规修订即是针对CLP法规新增的致癌、致突变或生殖毒性(CMR)物质,预备将其同步纳入化妆品禁用组分。
欧盟化妆品法规拟修订内容如下:
修订附录Ⅱ
a. 新增条目:
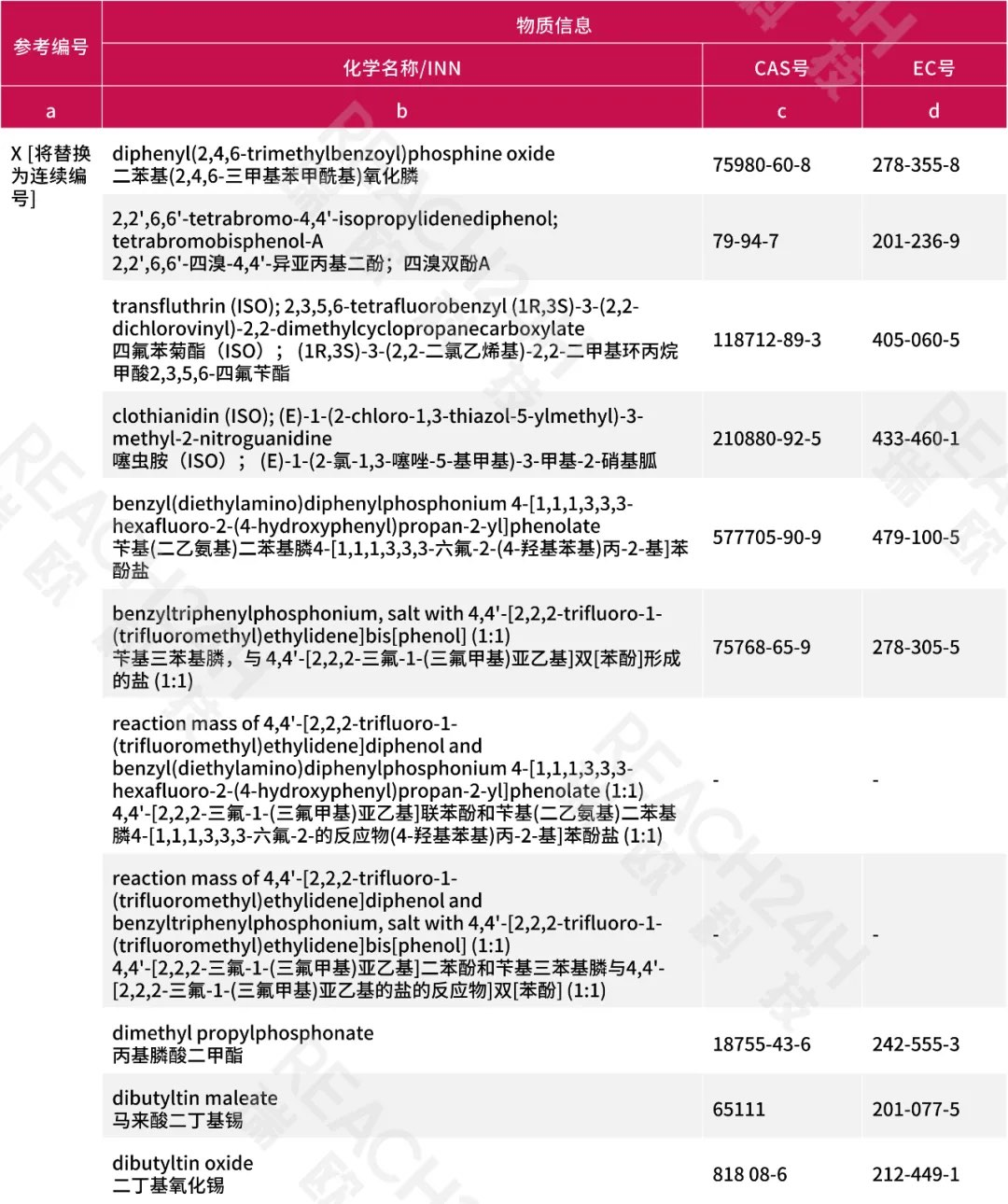
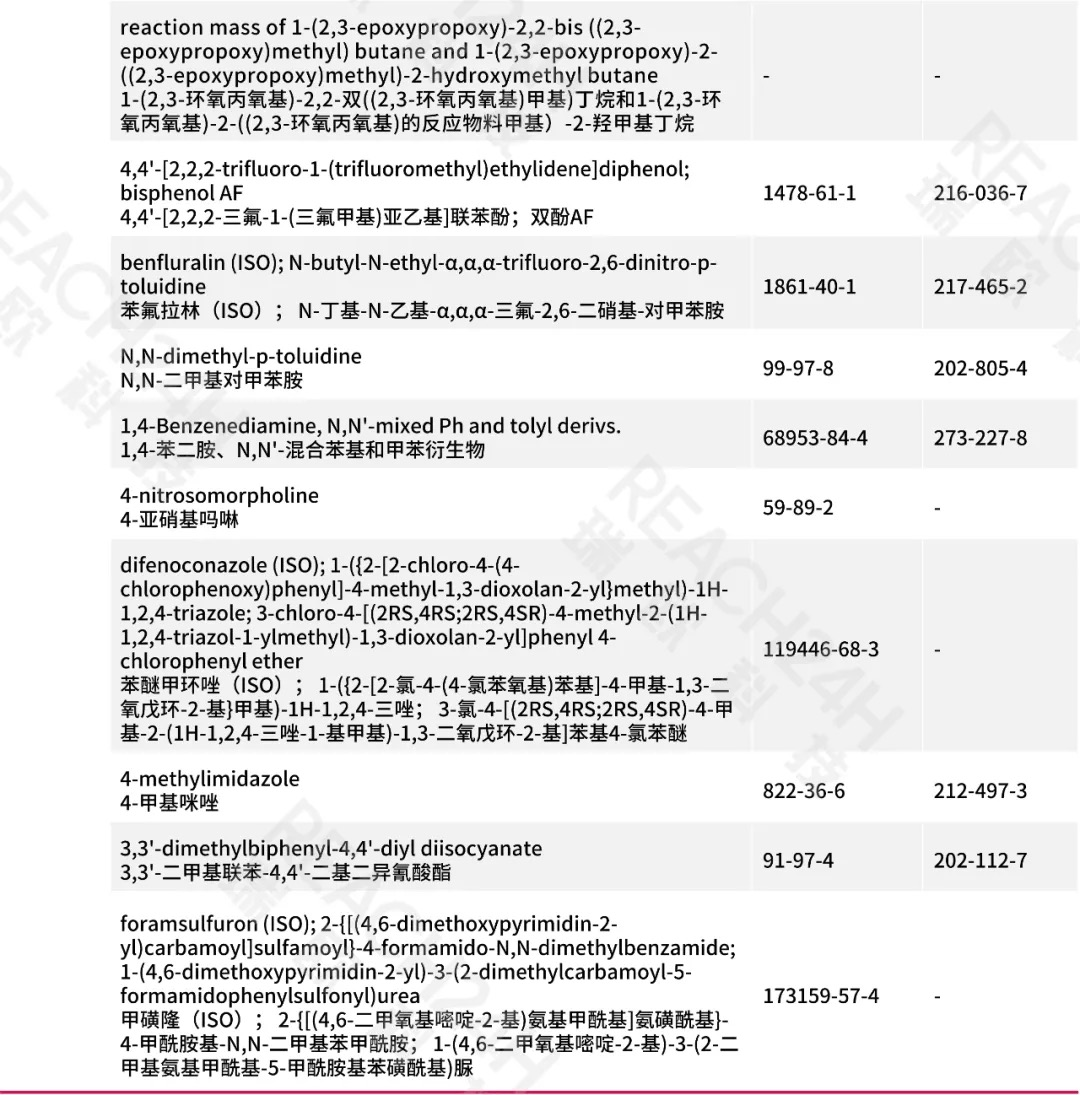
b. 原第1580条替换为:

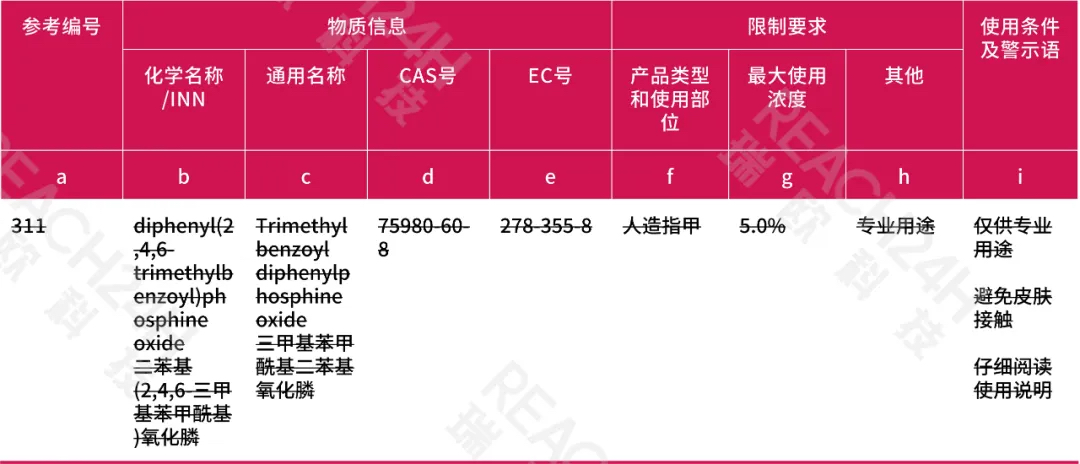
修订附录Ⅲ
删除第311条
来源:瑞欧科技
凡注明“来源:XXX”的文章,均转载自其它媒体,转载目的在于传递更多的信息,并不代表本网赞同其观点和对其真实性负责。如因文章内容、版权等其他问题,请同本网联系。






